Il parere del Comitato nazionale di bioetica sull’utilizzo dei bloccanti per la pubertà per i minorenni
Dice che servono più studi per capirne meglio gli effetti, ma una parte dei suoi membri si è detta generalmente contraria a queste terapie
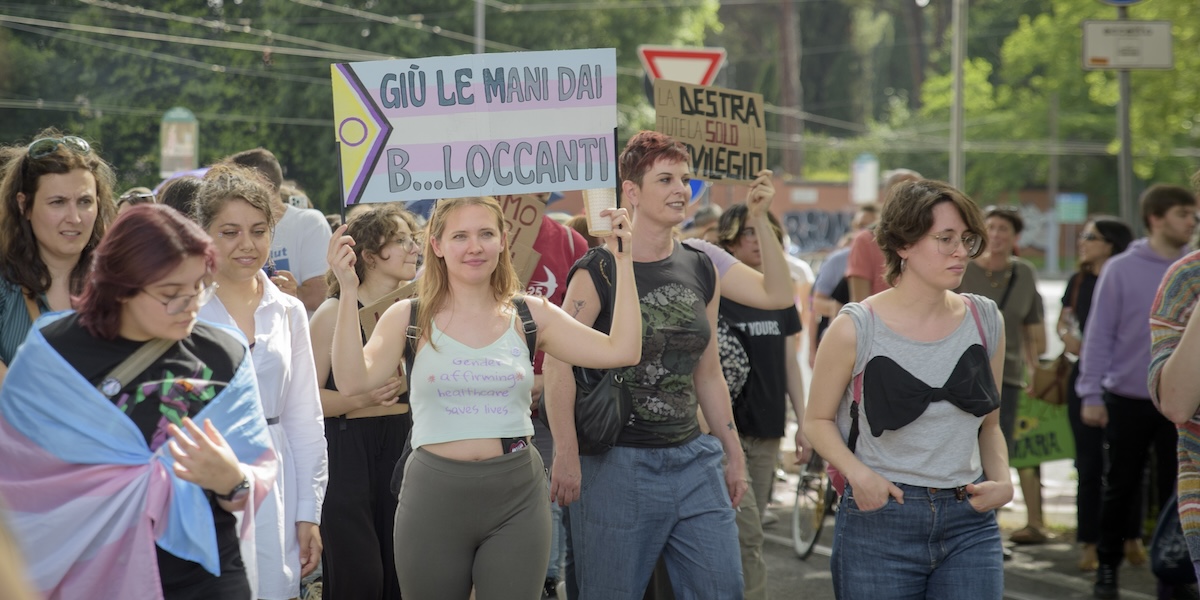
Il Comitato nazionale di bioetica (CNB), un organo consultivo del governo che si occupa di questioni scientifiche particolarmente complesse dal punto di vista etico e giuridico, ha consigliato che vengano finanziati più studi clinici indipendenti per raccogliere maggiori dati riguardo agli effetti e al rapporto costi/benefici dei cosiddetti “farmaci bloccanti per la pubertà”, utilizzati nei trattamenti per la disforia di genere nei minorenni che non si identificano col genere corrispondente al proprio sesso biologico.
Il Comitato, il cui parere non è vincolante, era stato interpellato dal ministero della Salute perché si esprimesse sull’opportunità o meno, dal punto di vista etico, di somministrare ai minorenni la triptorelina, il farmaco che sospende alcuni aspetti dello sviluppo puberale. I bloccanti della pubertà sono utilizzati in vari paesi, compresa l’Italia, per accompagnare il percorso di adolescenti e preadolescenti che non si sentono a proprio agio nel genere associato al loro sesso biologico. Da alcuni anni però questi farmaci sono al centro di un esteso e acceso dibattito, e di recente sono stati vietati a tempo indeterminato nel Regno Unito, dopo la pubblicazione di un atteso rapporto dal quale emergevano delle lacune nelle conoscenze scientifiche sui loro effetti.
Nel parere appena pubblicato (consultabile qui) il Comitato ha detto di essere giunto a queste conclusioni dopo una serie di audizioni con esperti e dopo aver valutato la letteratura scientifica disponibile. Il parere è stato pubblicato con 29 voti favorevoli, 2 astensioni e 1 voto contrario. Quasi all’unanimità, quindi: è un dato notevole, tenendo conto che il Comitato è composto da persone con orientamenti, visioni e livelli di competenza molto diversi, e che il tema è molto divisivo e polarizzante.
– Leggi anche: Perché si discute di bloccanti per la pubertà e transizione di genere nei più giovani
I dubbi del ministero della Salute riguardavano soprattutto il livello di consapevolezza che persone così giovani hanno nel momento in cui acconsentono a iniziare trattamenti così impattanti sul proprio corpo. A questo proposito, il Comitato ha allegato una dichiarazione di voto firmata da 15 membri che, pur aderendo al parere generale del Comitato sulla necessità di migliorare la nostra comprensione degli effetti dei farmaci bloccanti per la pubertà, si sono detti eticamente contrari a permettere a persone minorenni di intraprendere un percorso di transizione di genere. Secondo i membri del Comitato che hanno sottoscritto questa dichiarazione, «molti dei cambiamenti fisici previsti e intrapresi sono irreversibili, e la compromissione della fertilità risulta spesso inevitabile».
Nel parere appena pubblicato, il Comitato ha detto che gli studi da svolgere devono essere «di qualità superiore a quelli già realizzati», che ritiene non adatti a poter rispondere alla domanda rivolta dal governo. Il Comitato ha definito «carenti e frammentari» anche i dati disponibili sull’utilizzo della triptorelina nelle varie Regioni italiane.
A tal proposito, il Comitato ha ricordato che il modello di riferimento per gli studi clinici da svolgere è quello dello «studio controllato e randomizzato in doppio cieco». È un tipo di studio in cui i partecipanti vengono assegnati in maniera casuale a due gruppi, il gruppo sperimentale che riceve il trattamento e quello che non lo riceve, per poter confrontare i risultati, e in cui sia gli sperimentatori che i partecipanti non conoscono il tipo di trattamento assegnato. Sono tutti criteri pensati per rendere il più imparziale e obiettiva possibile una sperimentazione, evitando che aspettative consce o inconsce influenzino la sua valutazione.
Il Comitato ha inoltre raccomandato che eventuali prescrizioni di questo farmaco vengano effettuate in maniera controllata, possibilmente all’interno di sperimentazioni promosse dallo stesso ministero della Salute, e comunque seguendo gli stessi criteri anche in eventuali prescrizioni esterne alle sperimentazioni cliniche. In linea generale, il Comitato ha detto che l’eventuale somministrazione della triptorelina dovrebbe avvenire solo dopo aver dimostrato l’inefficacia di altri tipi di terapie e percorsi meno impattanti dal punto di vista fisico, per esempio percorsi psicologici, psicoterapeutici o eventualmente psichiatrici, documentando tutti i passaggi del processo decisionale.
Come detto il parere del CNB non è vincolante: starà ora al governo decidere se e come far partire e finanziare nuovi studi clinici sull’utilizzo della triptorelina, in maniera da guadagnare le conoscenze necessarie per rispondere alla domanda che aveva rivolto al Comitato.
Il Comitato ha accompagnato il proprio parere con due note in cui chi ha votato in maniera contraria e chi si è astenuto ha argomentato le proprie posizioni, e da due dichiarazioni di voto. Nella seconda dichiarazione i 7 membri firmatari hanno enfatizzato l’importanza di acquisire conoscenze sull’utilizzo della triptorelina e di creare strumenti per poter seguire lo sviluppo dei suoi effetti e di quello che si scoprirà in futuro, per esempio attraverso l’istituzione di un registro nazionale centralizzato sul suo utilizzo.