Le indagini sull’omeopatia negli Stati Uniti
La Food and Drug Administration sta concludendo una lunga consultazione sulla sua efficacia e potrebbe introdurre regole più severe per i produttori
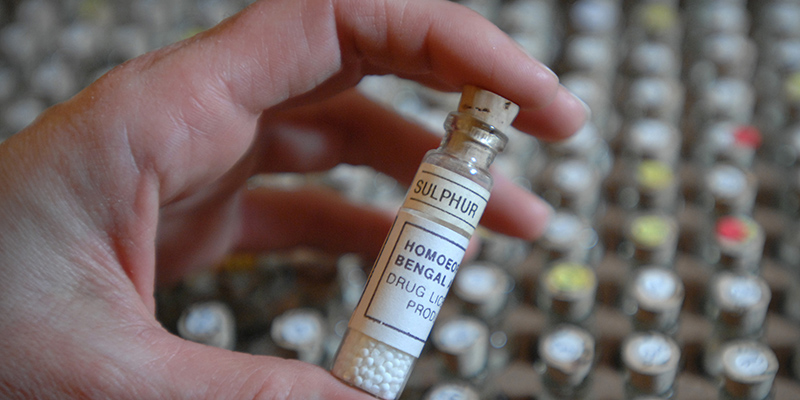
Negli Stati Uniti la Food and Drug Administration (FDA), l’agenzia del governo che si occupa di regolamentare farmaci e prodotti alimentari, sta concludendo una lunga consultazione avviata a inizio anno sull’omeopatia, il controverso sistema che secondo i suoi sostenitori serve a “curare” dalle malattie utilizzando dosi estremamente diluite di ciò che causa i sintomi nelle persone malate.
L’iniziativa della FDA potrebbe portare a una revisione delle etichette riportate sui prodotti omeopatici per distinguerli meglio dai farmaci veri e propri, dopo anni in cui erano stati sostanzialmente ignorati dall’agenzia statunitense. Criticata da tempo da medici e ricercatori, l’omeopatia è stata definita inefficace per il trattamento di qualsiasi patologia lo scorso marzo dal National Health and Medical Research Council, il più importante istituto australiano di ricerca medica, sulla base di oltre 255 studi scientifici pubblicati negli ultimi anni sulle pratiche omeopatiche.
Rischi
Molto diffusi in alcuni paesi europei, i prodotti omeopatici hanno un mercato sempre più consistente anche negli Stati Uniti: le stime più recenti, riferite al 2013, parlano di volumi di vendita intorno ai 6,4 miliardi di dollari per i rimedi di questo tipo. Proprio le dimensioni del mercato e i nuovi studi molto critici circa la sua efficacia hanno spinto l’FDA ad analizzare meglio l’omeopatia, in vista dell’introduzione di regole più rigide. Oltre a essere ritenuti inefficaci per la cura delle malattie, i prodotti omeopatici possono causare seri problemi alla salute. La stessa FDA solo nel 2009 ha ricevuto più di 130 segnalazioni da parte di pazienti che avevano perso la capacità di riconoscere gli odori in seguito all’assunzione di un prodotto omeopatico a base di zinco. L’anno seguente l’agenzia dovette invece fare i conti con un tipo di pastiglie omeopatiche – vendute come “prodotto naturale al 100 per cento” – che causavano seri effetti collaterali nei bambini.
Come gli alimentari
Finora i prodotti omeopatici negli Stati Uniti non sono stati sottoposti a particolari controlli, a differenza dei farmaci tradizionali che devono superare una enorme serie di test e prove cliniche molto costosi prima di essere approvati e messi in vendita. La FDA verifica unicamente che gli omeopatici siano prodotti in ambienti puliti e sicuri, come fa del resto per gli alimenti in generale, ma non si occupa di valutare l’efficacia dei trattamenti eventualmente indicata sulle etichette. Il controllo è quindi molto blando e di gran lunga inferiore rispetto ad altri prodotti da banco venduti in farmacia, come gli integratori alimentari e le vitamine, cui sono imposti limiti circa le dichiarazioni sui loro effetti indicati nelle etichette.
La FDA ha dato tempo fino a oggi alle parti interessate (produttori, consumatori, medici, ricercatori) per inviare i loro commenti, dopodiché i responsabili dell’agenzia tireranno le loro conclusioni con l’eventuale introduzione di nuove regole. Cercando di venire incontro alla FDA e di evitare norme troppo severe, alcuni produttori di omeopatici hanno detto di essere disposti a rivedere il modo in cui sono fatte le etichette, aggiungendo per esempio una dicitura in cui si specifica che i loro prodotti non sono stati testati dalla FDA. Altri propongono di eliminare le diciture in latino con il nome dei composti che si trovano all’interno di soluzioni e pillole, in forme enormemente diluite.
Cos’è l’omeopatia
Le teorie legate ai principi omeopatici furono elaborate dal tedesco Samuel Hahnemann agli inizi del XIX secolo: dicono che la salute di ogni persona è dovuta a una sorta di “energia vitale immateriale”, che provvede ad armonizzare le varie parti dell’organismo. Secondo Hahnemann per curare una malattia bisogna utilizzare una medicina che produca nell’organismo una specie di malanno artificiale, simile a quello di cui soffre già il paziente; la malattia indotta deve sostituirsi a quella già esistente e poi deve scomparire. Il trattamento prevede l’utilizzo di dosi infinitesimali della sostanza, che viene diluita decine di volte in una sostanza neutra, acqua (con una percentuale di alcol) o zucchero, nel caso dei preparati solidi. Se sull’etichetta c’è scritto 15C, significa che la sostanza è stata diluita 15 volte in 99 parti diluenti, per un totale di 10015. La diluizione nei prodotti omeopatici è tale da rendere praticamente impossibile che la sostanza possa avere un minimo effetto su chi assume questo tipo di prodotti, hanno spiegato in più occasioni diverse ricerche scientifiche.
Alcol
I prodotti omeopatici possono comunque indurre diversi effetti, a volte legati alle altre sostanze “inattive” presenti nella diluizione. Yvette d’Entremont ha raccontato di recente su Slate come è riuscita a ubriacarsi bevendo alcune boccette di un prodotto omeopatico che, secondo le indicazioni sull’etichetta, sarebbe dovuto servire contro la stipsi. Il prodotto era costituto al 20 per cento da etanolo, come un blando liquore, ma era normalmente venduto in farmacia e senza particolari limitazioni per i minorenni, che per esempio non possono acquistare alcolici fino ai 21 anni nella maggior parte degli Stati Uniti.
Leggi
Le vicende dei prodotti omeopatici negli Stati Uniti si intrecciano con le leggi via via approvate dal Congresso. Nel 1938 furono aggiunti agli elenchi dei normali farmaci, e negli anni seguenti ebbero sempre meno successo perché disponibili solo per la vendita presso gli ambulatori degli omeopati. Le cose cambiarono nel 1988 quando una nuova legge consentì la vendita di questi prodotti sugli scaffali delle farmacie, senza la necessità di presentare una ricetta medica. Negli anni le loro confezioni sono diventate sempre più simili a quelle degli altri farmaci, e il fatto che siano spesso esposte insieme ai medicinali veri e propri confonde i consumatori, che pensano di potere ottenere gli stessi risultati con un prodotto omeopatico riducendo gli effetti collaterali.
La FDA non è comunque l’unica agenzia federale statunitense ad avere avviato nuove verifiche sugli omeopatici. La Federal Trade Commission (FTC), che si occupa della tutela dei consumatori e della libera concorrenza, a fine agosto ha pubblicato un documento in cui solleva diversi dubbi sull’omeopatia, invitando la FDA a regolamentare meglio il mercato dei prodotti omeopatici “che possono causare danni ai consumatori”.
In Italia i prodotti omeopatici possono essere venduti solo in farmacia. La spesa per il loro acquisto è interamente a carico dei clienti: non sono previste convenzioni dirette con il Servizio sanitario nazionale, ma ogni Regione ha la facoltà di includerle sulla base di vari criteri.



