Ci sono novità sul farmaco che riduce il rischio di contrarre l’AIDS
Una commissione di esperti ne ha consigliato l'adozione alle autorità statunitensi, che decideranno a giugno
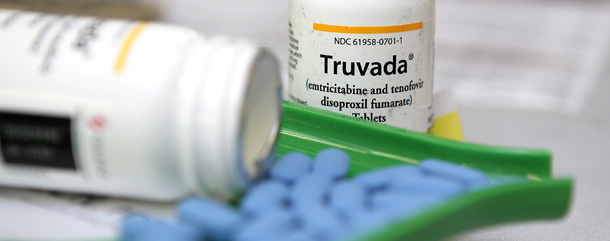
Per la prima volta nella sua storia, l’Antiviral Drugs Advisory Committee (AVAC) ha consigliato alle autorità sanitarie statunitensi di approvare il Truvada come farmaco per prevenire l’AIDS, e non solo come terapia per tenere sotto controllo la malattia come è stato impiegato fino a ora. L’AVAC è una commissione che fa parte della Food and Drug Administration (FDA), l’agenzia governativa che negli Stati Uniti si occupa della regolamentazione dei prodotti farmaceutici e alimentari. Il parere della commissione non è vincolante per la FDA, che darà il proprio parere a metà giugno, ma segna un importante passo avanti per i sistemi di prevenzione dell’AIDS.
L’AVAC si è occupata del Truvada, un farmaco prodotto dalla società farmaceutica californiana Gilead Sciences, in seguito a una serie di studi che nel 2010 dimostrarono l’efficacia del medicinale nel ridurre il rischio di contrarre il virus dell’HIV, che provoca l’AIDS. Una ricerca, pubblicata sulla rivista scientifica New England Journal of Medicine e condotta su centinaia di uomini omosessuali, dimostrò che il Truvada aveva ridotto del 44 per cento la probabilità di rimanere infettati dal virus rispetto al gruppo di controllo che assumeva un placebo.
Il Truvada è nato dalla combinazione di due principi attivi già commercializzati, il Tenofovir e l’Emtricitabina. Il farmaco agisce colpendo il virus dell’AIDS nel sangue e non a livello locale, come fanno per esempio i gel microbicidi vaginali. Non ha particolari effetti collaterali, anche se in alcuni casi può causare temporanei mal di testa e nausea e con pazienti in particolari condizioni anche problemi renali. Il Truvada è già prescritto in alcuni paesi, ma principalmente come aiuto nelle terapie per le persone che sono già malate di AIDS. Le scoperte del 2010 hanno reso il farmaco un valido candidato per diventare un medicinale per la profilassi pre-espositiva (PreP), ovvero somministrare il Truvada per prevenire la contrazione del virus nel caso in cui si venga in contatto con persone sieropositive.
Il farmaco dà un tipo di protezione che non richiede necessariamente il permesso da parte del partner, e dunque può essere utilizzato da chi si prostituisce, da chi potrebbe subire violenze sessuali per esempio in carcere o da chi riceve forti pressioni per non utilizzare il preservativo. Quando furono comunicati i primi risultati nel 2010, l’UNAIDS, l’agenzia delle Nazioni Unite che si occupa della lotta all’AIDS, confermò che la scoperta avrebbe presto consentito di accelerare i progressi nella prevenzione della malattia.
Negli Stati Uniti, e in altri paesi, il Truvada viene già prescritto da alcuni medici per la profilassi pre-espositiva, ma non esistono ancora protocolli ufficiali per eseguire le terapie che possono essere indicati solamente dagli organismi governativi di controllo. Per questo motivo i membri dell’AVAC si sono riuniti per analizzare i risultati fino a ora emersi sul Truvada e consigliare alla FDA la strada da seguire. La riunione non è stata per nulla semplice, hanno spiegato diversi membri della commissione, e l’incontro è durato per più di undici ore. Le principali obiezioni erano legate al fatto che l’approvazione di terapie di prevenzione con farmaci possano far abbassare la guardia ai soggetti a rischio, aumentando di fatto il rischio che questi contraggano l’AIDS.
L’AVAC ha votato a favore dell’utilizzo del Truvada come sistema per la PreP per tre distinti gruppi di pazienti: uomini che fanno sesso con altri uomini (19 sì e 3 no), coppie in cui uno dei partner è sieropositivo (19 sì, 2 no e una astensione) e gruppi di soggetti con particolari fattori di rischio (12 sì, 8 no e due astenuti). Negli Stati Uniti ogni anno contraggono l’AIDS circa 56mila persone e la maggior parte di queste sono di sesso maschile.
Secondo i detrattori, il Truvada difficilmente potrà essere una valida soluzione nella prevenzione. Per avere una buona protezione, occorre assumere il farmaco tutti i giorni e un anno di terapia costa intorno ai 14mila dollari. Perché sia efficace, ha spiegato una consulente durante la discussione dell’AVAC, il Truvada deve essere assunto con costanza, il cento per cento delle volte, cosa che è difficilissima da ottenere con i pazienti, specie se non sono assistiti e sottoposti a regolari controlli in clinica. Il parere della commissione non è vincolante e sarà preso in considerazione dagli esperti della FDA, che a metà giugno dovranno decidere se rendere o meno il Truvada un farmaco anche per la profilassi pre-espositiva.



